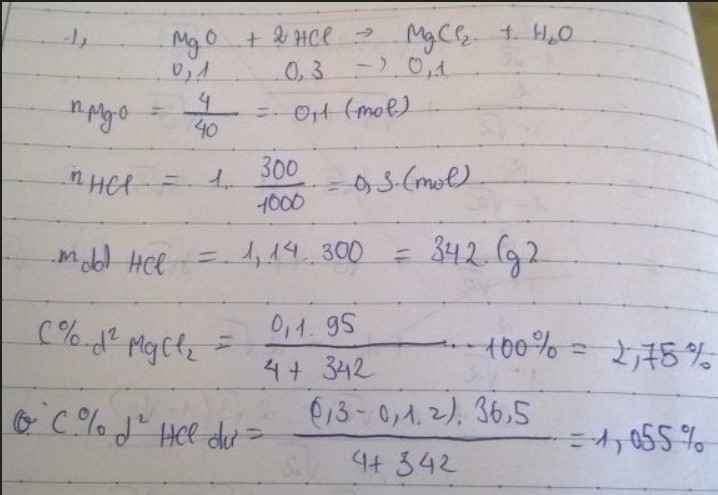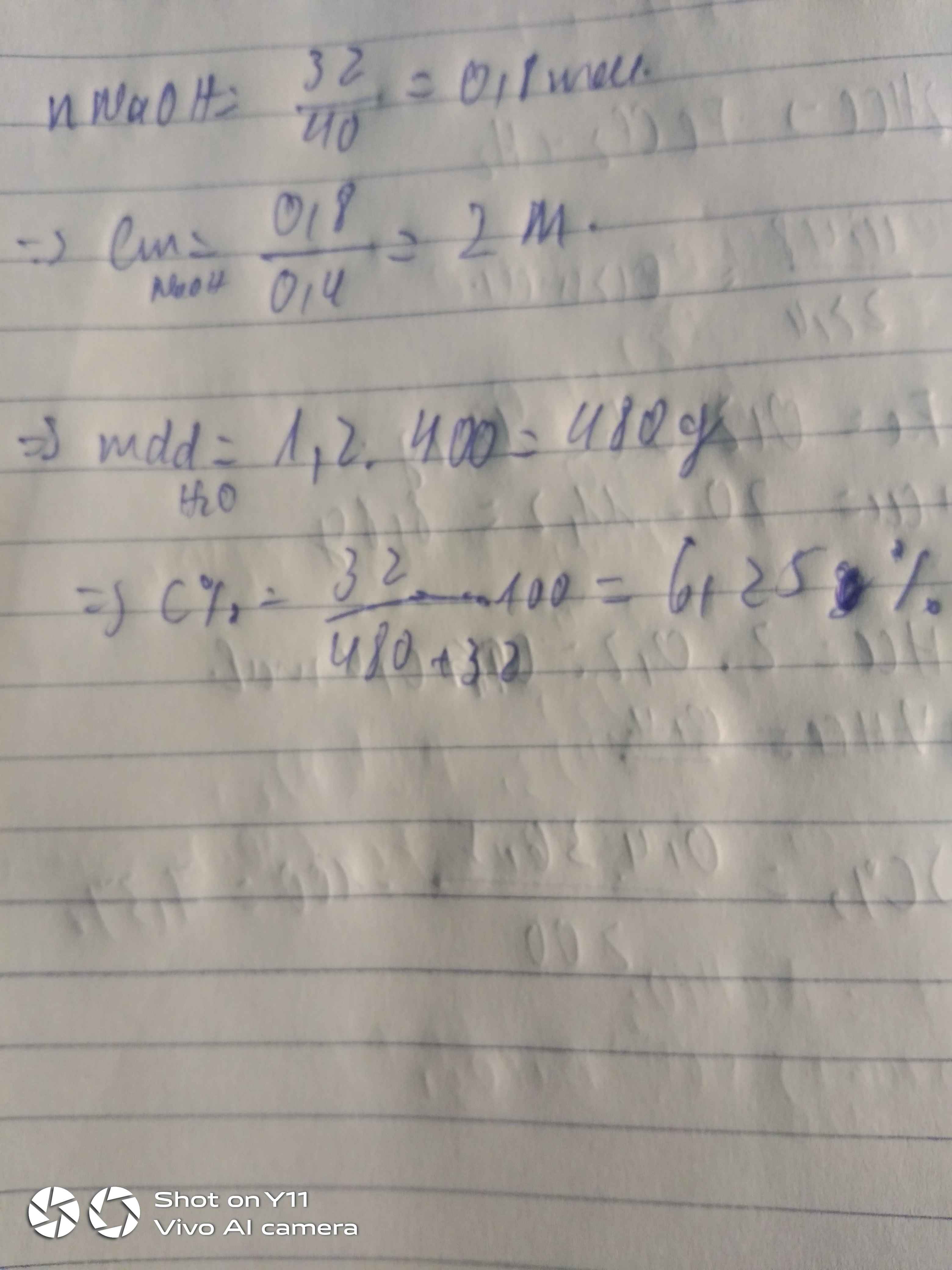Những câu hỏi liên quan
cho 2,7g bột nhôm vào 120ml dúng dịch CuSO4 10% có khối lượng riêng là 1,12g/ml
a, viết PTHH
b, xác định nồng độ mol của chất trong dung dịch khi phản ứng kết thúc. Giả thiết rằng thể tích của dung dịch sau phản ứng thay đổi không đáng kể
giúp mình vớiiii
a, \(2Al+3CuSO_4\rightarrow Al_2\left(SO_4\right)_3+3Cu\)
b, Ta có: \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
\(m_{ddCuSO_4}=120.1,12=134,4\left(g\right)\)
\(\Rightarrow n_{CuSO_4}=\dfrac{134,4.10\%}{160}=0,084\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,1}{2}>\dfrac{0,084}{3}\), ta được Al dư.
Theo PT: \(\left\{{}\begin{matrix}n_{Cu}=n_{CuSO_4}=0,084\left(mol\right)\\n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}n_{CuSO_4}=0,028\left(mol\right)\end{matrix}\right.\)
nAl (pư) = 2/3nCuSO4 = 0,056 (mol)
Ta có: m dd sau pư = 0,056.27 + 134,4 - 0,084.64 = 130,536 (g)
\(\Rightarrow C\%_{Al_2\left(SO_4\right)_3}=\dfrac{0,028.342}{130,536}.100\%\approx7,34\%\)
Đúng 2
Bình luận (0)
Cho 1,96g bột sắt vào 100ml dung dịch CuSO4 10% có khối lượng riêng là 1,12g/ml a) Viết PTHH b) Xác định nồng độ mol của chất trong dung dịch khi phản ứng kết thúc. Giả thiết rằng thể tích của dung dịch sau phản ứng thay đổi không đáng kể.
a) Phương trình phản ứng: Fe + CuSO4 → FeSO4 + Cu b) Số mol của Fe là : 1,96 : 56 = 0,035 (mol) Khối lượng dd CuSO4 là : m ddCuSO4 = 1,12 . 100 = 112 (g) Khối lượng CuSO4 có trong dd là :
mCuSO4 = 10% . 112 = 11,2 (g)
Số mol của CuSO4 là :
11,2 : 160 = 0,07 mol
Fe + CuSO4 ——> FeSO4 + Cu (1)
Theo (1) ta có : nFe = nCuSO4 = 0,07 mol > 0,035 mo
l => số mol của CuSO4 dư
Vậy ta tính theo số mol của Fe.
CM CuSO4 = (0,07 – 0,035/100)*1000 = 0,35 (M)
CM FeSO4 = (0,035/100)*1000 = 0,35 (M)
Đúng 1
Bình luận (0)
cho 1,96g bột sắt vào 100ml dung dịch CuSO4 10% có khối lượng riêng là 1,12 g/ml
a, viết PTHH
b, Xác định nồng độ mol của chất trong dung dịch khi phản ứng kết thúc. Giả thiết rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể
giúp mình với ạaa
a, \(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
b, \(n_{Fe}=\dfrac{1,96}{56}=0,035\left(mol\right)\)
\(m_{ddCuSO_4}=100.1,12=112\left(g\right)\)
\(\Rightarrow n_{CuSO_4}=\dfrac{112.10\%}{160}=0,07\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,035}{1}< \dfrac{0,07}{1}\), ta được CuSO4 dư.
Theo PT: \(n_{CuSO_4\left(pư\right)}=n_{FeSO_4}=n_{Cu}=n_{Fe}=0,035\left(mol\right)\)
\(\Rightarrow n_{CuSO_4\left(dư\right)}=0,07-0,035=0,035\left(mol\right)\)
Ta có: m dd sau pư = 1,96 + 112 - 0,035.64 = 111,72 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeSO_4}=\dfrac{0,035.152}{111,72}.100\%\approx4,76\%\\C\%_{CuSO_4}=\dfrac{0,035.160}{111,72}.100\%\approx5,01\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
1.cho 1,4g bột sắt vào 100ml dung dịch CuSO4 10% có khối lượng riêng là 1,12g/ml. Xác định nồng độ mol của chất tronh dung dịch khi phản ứng kết thúc. Giả thiết rằng thể tích của dung dịch sau phản ứng thay đổi không đáng kể2.nung hỗn hợp gồm 22.4 sắt và 8g lưu huỳnh trong môi trường không có không khí. Sau phản ứng thu được hỗn hợp chất rắn A. Cho dung dịch HCL 1M phản ứng vừa đủ với A thu được hỗn hợp khí B. Tính thể tích dung dịch HCL 1M đã tham gia phản ứng3. Tính thể tích dd NaOH 2M để tác...
Đọc tiếp
1.cho 1,4g bột sắt vào 100ml dung dịch CuSO4 10% có khối lượng riêng là 1,12g/ml. Xác định nồng độ mol của chất tronh dung dịch khi phản ứng kết thúc. Giả thiết rằng thể tích của dung dịch sau phản ứng thay đổi không đáng kể
2.nung hỗn hợp gồm 22.4 sắt và 8g lưu huỳnh trong môi trường không có không khí. Sau phản ứng thu được hỗn hợp chất rắn A. Cho dung dịch HCL 1M phản ứng vừa đủ với A thu được hỗn hợp khí B. Tính thể tích dung dịch HCL 1M đã tham gia phản ứng
3. Tính thể tích dd NaOH 2M để tác dụng hoàn toàn với 5,6list khí clo (đktc). Nồng độ mol của các chất sau phản ứng là bao nhiêu? Giả thiết thể tích dung dịch thay đổi không đáng kể
4. Cho 52,2g MnO2 tác dụng với dung dịch HCl đặc dư thu được một lượng khí X. Dẫn khí X vào 500ml dung dịch NaOH 3M thu được dung dịch A. Tính nồng độ mol của các chất trong dd A. Giả thiết rằng thể tích dd sau phản ứng thay đổi ko đáng kể
2.nung hỗn hợp gồm 22.4 sắt và 8g lưu huỳnh trong môi trường không có không khí. Sau phản ứng thu được hỗn hợp chất rắn A. Cho dung dịch HCL 1M phản ứng vừa đủ với A thu được hỗn hợp khí B. Tính thể tích dung dịch HCL 1M đã tham gia phản ứng
\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right);n_S=\dfrac{8}{32}=0,25\left(mol\right)\)
PTHH : Fe + S -------to------> FeS
Theo đề: 0,4.......0,25 (mol)
Lập tỉ lệ : \(\dfrac{0,4}{1}>\dfrac{0,25}{1}\)=> Sau phản ứng Fe dư
=> \(n_{Fe\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
Fe + 2HCl ------> FeCl2 + H2
FeS + 2HCl ------> FeCl2 + H2S
\(V_{HCl}=\dfrac{0,15.2+0,25.2}{1}=0,8\left(l\right)\)
Đúng 1
Bình luận (0)
1.cho 1,4g bột sắt vào 100ml dung dịch CuSO4 10% có khối lượng riêng là 1,12g/ml. Xác định nồng độ mol của chất tronh dung dịch khi phản ứng kết thúc. Giả thiết rằng thể tích của dung dịch sau phản ứng thay đổi không đáng kể
PTHH: Fe + CuSO4 → FeSO4 + Cu
\(n_{Fe}=\dfrac{1,4}{56}=0,025\left(mol\right)\)
m ddCuSO4 = 1,12 . 100 = 112 (g)
=> m CuSO4 = 10% . 112 = 11,2 (g)
=> \(n_{CuSO_4}=\dfrac{11,2}{160}=0,07\left(mol\right)\)
Theo PT, lập tỉ lệ nFe : nCuSO4 = \(\dfrac{0,025}{1}< \dfrac{0,07}{1}\) => CuSO4 dư sau phản ứng
\(CM_{CuSO_4\left(dư\right)}=\dfrac{0,07-0,025}{0,1}=0,45M\)
\(CM_{FeSO_4}=\dfrac{0,025}{0,1}=0,25M\)
Đúng 1
Bình luận (0)
3. Tính thể tích dd NaOH 2M để tác dụng hoàn toàn với 5,6list khí clo (đktc). Nồng độ mol của các chất sau phản ứng là bao nhiêu? Giả thiết thể tích dung dịch thay đổi không đáng kể
PTHH: 2NaOH + Cl2 → NaClO + NaCl + H2O
Theo PT: \(n_{NaOH}=2n_{Cl_2}=\dfrac{2.5,6}{22,4}=0,5\left(mol\right)\)
=> \(V_{NaOH}=\dfrac{0,5}{2}=0,25\left(l\right)\)
Theo PT: \(n_{NaClO}=n_{NaCl}=n_{Cl_2}=0,25\left(mol\right)\)
\(CM_{NaClO}=CM_{NaCl}=\dfrac{0,25}{0,25}=1M\)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Hòa tan hoàn toàn 4g NaOH có nồng độ 10% vào dung dịch CuCl2 có nồng độ 10% a) viết PTHH xảy ra b) Tính khối lượng dung dịch CuCl2 đã dùng c) tính nồng độ phần trăm (c%) của chất trong dung dịch sau phản ứng (Biệt Cu = 64 ; O = 16 ; Na = 23 ; Cl = 35,5 ; H=1)
\(a)2NaOH+CuCl_2\rightarrow Cu\left(OH\right)_2+2NaCl\\ b)n_{NaOH}=\dfrac{4}{40}=0,1mol\\ n_{CuCl_2}=n_{Cu\left(OH\right)_2}=0,1:2=0,05mol\\ m_{ddCuCl_2}=\dfrac{0,05.135}{10}\cdot100=67,5g\\ c)n_{NaCl}=n_{NaOH}=0,1mol\\ C_{\%NaCl}=\dfrac{0,1.58,5}{\dfrac{4}{10}\cdot100+67,5-0,05.98}\cdot100=14,0625\%\)
Đúng 1
Bình luận (0)
Bài 4. (3đ) Hòa tan hoàn toàn 4 gam MgO vào 300ml dung dịch HCl 1M.
1/ Viết phương trình hóa học xảy ra
2/ Tính nồng độ phần phần trăm(C %) của các chất có trong dung dịch sau khi phản ứng kết thúc. (Biết khối lượng riêng của dd HCl là D = 1,14g/ml)
Bài 4 :
\(n_{MgO}=\dfrac{4}{40}=0,1\left(mol\right)\)
300ml = 0,3l
\(n_{HCl}=1.0,3=0,3\left(mol\right)\)
1) Pt : \(MgO+2HCl\rightarrow MgCl_2+H_2O|\)
1 2 1 1
0,1 0,3 0,1
2) Lập tỉ số so sánh : \(\dfrac{0,1}{1}< \dfrac{0,3}{2}\)
⇒ MgO phản ứng hết , HCl dư
⇒ Tính toán dựa vào số mol của MgO
\(n_{MgCl2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{MgCl2}=0,1.95=9,5\left(g\right)\)
\(n_{HCl\left(dư\right)}=0,3-\left(0,1.2\right)=0,1\left(mol\right)\)
⇒ \(m_{HCl\left(dư\right)}=0,1.36,5=3,65\left(g\right)\)
\(m_{ddHCl}=1,14.300=342\left(g\right)\)
\(m_{ddspu}=4+342=346\left(g\right)\)
\(C_{MgCl2}=\dfrac{9,5.100}{346}=2,75\)0/0
\(C_{HCl\left(dư\right)}=\dfrac{3,65.100}{346}=1,05\)0/0
Chúc bạn học tốt
Đúng 0
Bình luận (0)
Cho 1,6g CuO tác dụng hết với dd sulfuric H2SO4 có nồng độ 20%.
a, Viết PTHH.
b) Tính khối lượng dung dịch H2SO4 đã phản ứng
c) Tính nồng độ % của các chất có trong dd sau khi phản ứng kết thúc.
CuO+H2SO4->CuSO4+H2O
0,02----------------0,02 mol
n CuO=1,6\80=0,02 mol
=>m CuSO4=0,02.160=3,2g
=>thiếu dữ kiện
Đúng 0
Bình luận (1)
Cho 32g NaOH vào nước được 400ml dd có khối lượng riêng D=1,2g/ml . Tính nồng độ mol và nồng độ phần trăm của dung dịch
a) Cho 2,25 gam hỗn hợp A gồm Al, Fe, Cu tác dụng với dung dịch HCl dư, sau khi phản ứng kết thúc thu được 1344 ml (đktc) khí và còn lại 0,6 gam chất rắn không tan. Tính % khối lượng mỗi kim loại trong A.
b) Hấp thụ hoàn toàn 1,344 lít SO2 ( đktc) vào 13,95 ml dung dịch KOH 28%, có khối lượng riêng là 1,147g/ml. Hãy tính nồng độ phần trăm các chất có trong dung dịch sau phản ứng
1) Ptpư:
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
Fe + 2HCl \(\rightarrow\) FeCl2 + H2
Cu + HCl \(\rightarrow\) không phản ứng
=> 0,6 gam chất rắn còn lại chính là Cu:
Gọi x, y lần lượt là số mol Al, Fe
Ta có:
3x + 2y = 2.0,06 = 0,12
27x + 56 y = 2,25 – 0,6 = 1,65
=> x = 0,03 (mol) ; y = 0,015 (mol)
=> \(\%Cu=\frac{0,6}{2,25}.100\%=26,67\%\); \(\%Fe=\frac{56.0,015}{2,25}.100\%=37,33\%\); %Al = 36%
2) \(n_{SO_2}=\frac{1,344}{22,4}=0,06mol\); m (dd KOH) = 13,95.1,147 = 16 (gam)
=> mKOH = 0,28.16 = 4,48 (gam)=> nKOH = 0,08 (mol)=> \(1<\)\(\frac{n_{KOH}}{n_{SO_2}}<2\)
=> tạo ra hỗn hợp 2 muối: KHSO3: 0,04 (mol) và K2SO3: 0,02 (mol)
Khối lượng dung dịch sau pu = 16 + 0,06.64 = 19,84 gam
=> \(C\%\left(KHSO_3\right)=\frac{0,04.120}{19,84}.100\%\)\(=24,19\%\)
\(C\%\left(K_2SO_3\right)=\frac{0,02.158}{19,84}.100\%\)\(=15,93\%\)
Đúng 0
Bình luận (1)